Výzkum střevního mikrobiomu v poslední dekádě doslova explodoval. Gastrointestinální trakt (GIT) byl dlouho považován pouze za trávící orgán, nové technologie nás přivedly k poznání, jaký dopad má střevní mikrobiom na naše zdraví a nemoci. Víme o jeho úloze v metabolismu, imunitním systému a o jeho vlivu na chování.
Víme také o jeho změnách po porodu, změnách přicházejících s věkem v průběhu života, změnách souvisejících s charakteristikami prostředí, se stresem, se zdravotním stavem a s podávanými léky. Je toho dost, co o něm víme a nepochybně mnohem víc je toho, co o něm ještě nevíme. (1, 2)
V našem břiše žije a také usilovně pracuje na váhu něco kolem půldruhého kilogramu, na počet 1014 (tedy deset na čtrnáctou) nejrůznějších mikrobů, virů, kvasinek, hub, plísní, parazitů (jimž zřejmě bude nutné začít říkat slušněji; dodáváním vajíček parazita tenkohlavce prasečího se pokoušejí vědci experimentálně léčit střevní záněty, astma a dokonce autismus) a dalších malých tvorů, jejichž úkolem je pomoci nám při zapracování potravy a u toho vyrobit celou spoustu enzymů, které tělo nemá, také vyrobit něco mezi 70-90 % nejrůznějších neurotransmiterů a dalších působků včetně posvátné molekuly serotoninu, včetně „endozepinů“, usilovně posilovat imunitu jak navenek, tak uvnitř a mezi sebou navzájem. Polovic hmotnosti naší denní stolice tvoří tyto odumřelé mikroorganismy, které zde můžeme detekovat v posledních letech díky vývoji sekvenování u příležitosti zkoumání lidského genomu. Ten už je prozkoumán a v současné době běží výzkum zaměření na jejich mapování řízený National Institute of Health (NIH) v USA nazvaný Human Microbiome project.
Celá tahle zoologická zahrada se nazývá bakteriom, nebo ji také najdeme pod pojmem „bakteriota“ a má několiksetkrát více genů, než naše DNA. Hádka o to, zda je jich desetkrát víc než všech buněk v těle byla nakonec vyřešena ve prospěch našeho organismu (aby nás třeba mikrobiom nepřepral), a to tak, že při prvním sčítání buněk nebyly do celkového počtu zavzaty erytrocyty. Když se tak stane, dostáváme se s mikrobiomem na celkem vyrovnanou úroveň. Ale nejsem si jist, jak do toho zasáhnou mikroby z ostatních sliznic a povrchů včetně kůže.
Přesto má „vnitřní mozek“ (zvaný gut brain, nebo ENS) – s vlastní reflexní aktivitou a tedy nezávislý na autonomním nervovém systému (ANS) – docela slušný výkon, protože k tomu, co dosud bylo uvedeno, je třeba připočíst skutečnost, že ve stěně tenkého střeba jsou umístěny nervové pleteně obsahující stejný počet neuronů, jaký má mícha, tj. asi stot milionů a že jsou zde také nejrozsáhlejší části imunitního systému. Pokud jde o výkon střevního mozku, nezaměřuje se ani na filosofii, ani na logiku, ale mocně přispívá k prožitkům a pokynům našeho emočního světa. Zde pociťujeme „gut feelings“, označované někdy jako intuice.
Když si navíc uvědomíme, že to co je ve střevě, intraluminální obsah, je vlastně vně organismu a že to, co z toho bude vstřebáno, co ne a co bude eventuálně do střeva vyloučeno, určuje jedna vrstva epitelu, je jasné, že její buňky potřebují mocné pomocníky. A těmi jsou jak složky mikrobiomu, tak imunitní systém. Jednou z komplikací může být hyperpermeabilita střevní stěny, tzv. „leaky gut“, kdy mezery mezi jednotlivými buňkami, které jsou standardně jen několik angströmů se rozšíří a tudy do organismu pak mohou pronikat nežádoucí látky, nebo naopak z organismu unikat voda, jak se děje například při cholerové infekci.
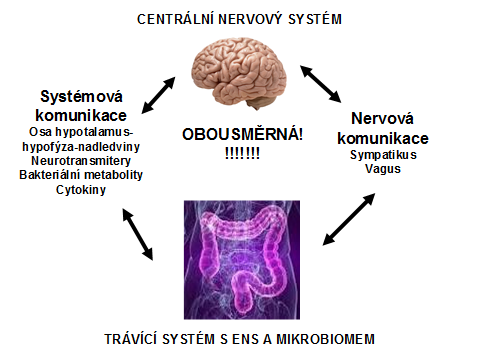
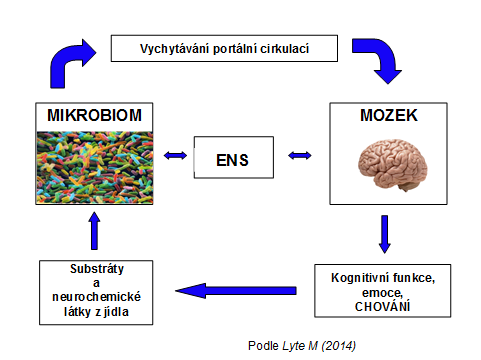
Komunikace s centrálním nervovým systémem je zajiš´tována jednak prostřednictvím nervu vagu, jehož 90 % vede odtud informace k mozku, jednak neurotransmitery putujícími krevním oběhem. Aby těch převratných novinek nebylo málo, je nutno zmínit také to, že před necelými dvěma roky padl mýtus o imunitní izolaci mozku. V mozkových plenách byly totiž objeveny mízní cévy zajišťující propojení s celým tělesným systémem.(3). Celý řídící systém je tedy mnohem dokonaleji propojený, než jsme si dosud představovali a mnohem komplexnější.
Jak jsme ke střevnímu mikrobiomu přišli? Dávno, pradávno a proto jsou také naši mrňaví pomocníci nazýváni „staří přátelé“. Kolonizace je věcí evoluce a charakteristické složení bakteriomu nacházíme u všech savců. Howard Ochman zmapoval vývoj bakteriomu velkých opic a říká, že jejich evoluci můžete pohodlně sledovat jen tím, že sledujete jejich bakteriom. Bakteriomy dvou druhů goril jsou si vzájemně bližší, než je jim blízký bakteriom člověka. Nicméně zachovávají si stále svou pestrost, biodiverzitu, zatímco tato charakteristika se u člověka stává stále chudší. (4) Pikantní je, že medvěd panda, který je šelma medvědovitá, se živí listím, kterého spořádá kolem 30 kg denně a má tedy v trávícím systému mikrobiom, umožňující mu tuto potravu zpracovat a využít. Dá se říci, že ač medvěd, má mikrobiální osazení trávícího systému podobné spíš krávě než jiným medvědům. Člověk se naopak vydal po cestě blížící se masožravcům.
Každý z nás má svůj specifický střevní mikrobiom, relativně stálý a podle charakteru mikrobiomu v ústech lze odhadnout jeho složení. A pozor, z ústního mikrobiomu je také možné usuzovat na riziko ICHS . Hlavní složkou střevního mikrobiomu jsou bakterie dvou základních typů, Firmicutes (nazvané tak podle pevného povrchu – firmus + cutis) a Bacteroidetes, které tvoří dohromady kolem 90 % populace. Mezi nimi jsou jak bakterie „hodné“, tak potenciální patobionti jakými jsou Clostridie, Helicobacer pylori, Mycobacteria a další. 10 % tvoří pestrá směs, čím pestřejší, s velkou biodiverzitou, tím zdravější. Podle dosavadních poznatků existuje mezi jednotlivými osadníky tenkého i tlustého střeva jakési ozbrojené příměří, jehož výsledkem je, že se žádný z nic nemůže jednostranně prosadit a vyvolat – v důsledku vzniklé nerovnováhy – značný dyskomfort až manifestní onemocnění. To se ale může snadno stát dojde-li k dysmikrobióze, tedy je-li tato rovnováha výrazně narušena nadbytkem některého druhu, častěji však jeho nedostatkem. Nejčastější příčinou takového nedostatku jsou enormně používaná a zneužívaná antibiotika v období posledních padesáti let a změněná strava.
Jak se zdá, ani plod v děloze není zcela prost mikrobů, ale není jich tam zase příliš. Na jejich existenci se usuzuje z různého složení mekonia v závislosti na době předčasného porodu a porodu v termínu. Hlavní porci tvořící základ budoucího mikrobiomu obdrží novorozenec při putování porodními cestami od matky – jsou to tedy kmeny obsažené v jejím vaginálním mikrobiomu a je nanejvýš pravděpodobné, že si také nabere něco málo z její stolice. To vše v případě, že je porod veden klasickým způsobem.
Při porodu císařským řezem tenhle mechanismus chybí a je proto logické, že – pokud porod neprobíhá v přísně aseptickém prostředí – je novorozenec „obdarován“ bakteriální směsí z porodního sálu, což není příliš výhodné, protože tato směs obsahuje kdeco, především stafylokoky, nemluvě o těch nebezpečnějších. Důsledkem toho je založení vlastního mikrobiomu, který není zcela optimální, což se pak dává do souvislosti s význemně vyšším výskytem alergií, atopií a též dalších autoimunitních problémů až po střevní záněty, obezitu, diabetes nebo roztroušenou sklerózu.
Některá pracoviště už problematiku řeší tak, že při císařském řezu porodníci vkládají tampon do vaginy rodičky a ten pak vkládají do úst novorozenci a potírají jím jeho tělíčko.
Na tomto místě se dostáváme celkem logicky ke gnotobiologii, což je obor, který se věnuje zkoumání bezmikrobních živočichů. Je to model umožňující sledovat funkci jednotlivých elementů bakteriomu na základě jejich vyřazení, ev. částečného dodatečného dodání některých jeho prvků. Ukazuje se například, že bezmikrobiální (germ-free) myši jsou motoricky mnohem aktivnější a vykazují méně úzkosti než jejich standardním mikrobiomem vybavené kamarádky. Zde začíná výzkum o vlivu mikrobiomu na lidské chování, který u zvířat už dává některé odpovědi, jež ale zatím nelze mechanicky aplikovat na člověka.
Jisté analogie tu ale přece jen jsou. Když do střev bezmikrobiálních myší vložíme mikrobiom z obezních zvířat, začnou při stejném složení stravy přibírat na hmotnosti. U lidí se už také prokazuje, že nelze jen mechanicky počítat kalorie/jouly, ale že je nutné také kalkulovat s tím, jak bude potrava zpracována a využita a to závisí od mikrobiomu. Tedy: nejste to, co jíte vy, ale jste tím, co jedí vaše bakterie.
Autor: MUDr. Radkin Honzák, CSc.
Literatura
(1) Collen A: 10 % člověka. Dobrovský (knihy Omega), Praha, 2015
(2) Perlmutter D: Brain maker. Yellow Kite, London, 2015
(3) Louveau A, Smirnov I, Keyes TJ, et al.: Structural and functional features of central nervous system lymphatic vessels. Nature. 2015;523(7560):337-341
(4) Moeller AH, et al.: Rapid changes in the gut microbiome during human evolution. Proc Natl Acad Sci U S A. 2014;111(46):16431-5
(5) Lyte M: Microbial endocrinology: Host-microbiota neuroendocrine interactions influencing brain and behavior. Gut Microbes, 2014;(5):381-389,2014























